[ad_1]
On pense que les informations contenues dans le cerveau sont codées sous forme de modèles complexes d’impulsions électriques générées par des milliers de cellules neuronales. Chaque impulsion, appelée potentiel d’action, est médiée par les courants d’ions chargés traversant la membrane d’un neurone.. Mais la façon dont les ions traversent la membrane isolée du neurone est restée un puzzle pendant de nombreuses années. En 1976, Erwin Neher et Bert Sakmann, qui ont définitivement montré que les courants résultaient de l’ouverture de nombreuses protéines du canal dans la membrane.. Bien que la technique ait été conçue à l'origine pour enregistrer des courants infimes, elle est depuis devenue l'un des outils les plus importants en neuroscience pour l'étude des signaux électriques – de l'échelle moléculaire au niveau des réseaux de neurones.
Dans les années 1970, il était généralement admis que le courant traversant la cellule résultait de l’ouverture de nombreux canaux dans la membrane, bien que le mécanisme sous-jacent soit inconnu. À cette époque, le courant était généralement enregistré en empalant un tissu avec une électrode tranchante – une pipette à pointe très fine. Malheureusement, le signal ainsi enregistré était excessivement bruyant et seul le gros courant «macroscopique» – courant collectif médiatisé par de nombreux types de canaux – traversant le tissu pouvait être résolu.
En 1972, Bernard Katz et Ricardo Miledi, pionniers de la biologie des connexions synaptiques entre cellules, ont réussi à déduire du courant macroscopique certaines propriétés des canaux membranaires, mais seulement après un effort héroïque visant à exclure tous les facteurs confondants possibles. Le problème était que le courant macroscopique pouvait être influencé par des facteurs non directement liés à l'activité du canal, tels que la géométrie des cellules et les processus modulateurs régulant l'excitabilité des cellules. Le fait que les interprétations des caractéristiques macroscopiques actuelles reposent sur des hypothèses non vérifiées concernant les statistiques de l'activité des canaux individuels est également gênant.,. En dépit des analyses minutieuses de Katz et Miledi, le doute subsistait quant à la validité de leurs conclusions. Les données cruciales ont été obtenues par Neher et Sakmann en utilisant un patch clamp.
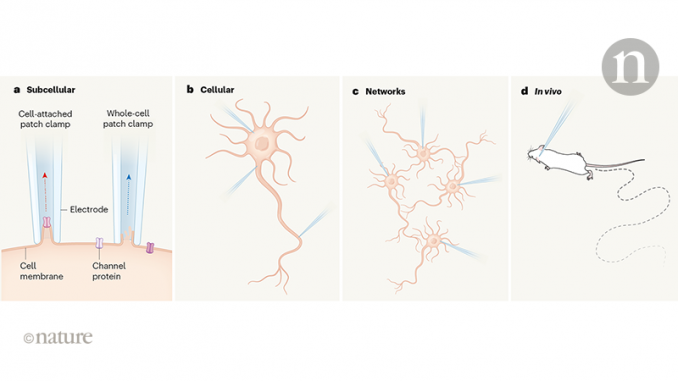
La technique du patch-clamp est conceptuellement plutôt simple. Au lieu d'empaler les cellules, une pipette de diamètre relativement grand est pressée contre la membrane cellulaire. Dans les bonnes conditions, la pointe de la pipette "se lie" à la membrane, formant ainsi un joint étanche. Ceci réduit considérablement le bruit par rapport à celui rencontré avec des électrodes tranchantes, car le petit morceau de membrane entouré par la pointe de la pipette est isolé électriquement du reste de la membrane de la cellule et de l’environnement environnant (Fig. 1).
Les faibles courants traversant les quelques canaux du patch ont ainsi été observés pour la première fois. L'enregistrement a confirmé les propriétés des canaux clés: lorsque les canaux s'ouvrent, il y a un saut semblable à un pas dans la trace en cours et, lorsqu'ils se ferment, un retour semblable à un pied revient à la ligne de base. Il était maintenant possible de déterminer des détails tels que les statistiques d'ouverture et de fermeture des canaux, l'amplitude des courants médiatisés et les stimuli optimaux qui déclenchent leur ouverture. Pour ce travail, Neher et Sakmann ont reçu le prix Nobel 1991 en physiologie ou médecine.
Les améliorations apportées au patch clamp ont rendu possible l’étude des canaux dans diverses préparations pour enfin répondre aux questions de longue date. Il y avait un intérêt particulier à vérifier un modèle de génération de potentiel d'action proposé par les lauréats du prix Nobel Alan Hodgkin et Andrew Huxley dans les années 1950. Les prévisions spécifiques du modèle pourraient maintenant être testées directement en examinant le courant par des canaux individuels et en observant les changements de courant qui se produisent lorsque la structure moléculaire du canal est modifiée.. En fin de compte, le modèle s’est révélé globalement correct et reste la norme de référence pour les neuroscientifiques en informatique.
Une des nombreuses variantes de patch clamp – la configuration de la cellule entière – a trouvé un public composé de neuroscientifiques étudiant les phénomènes électriques dans les neurones au-delà du niveau du canal. Pour réaliser un enregistrement de cellule entière, le patch de membrane situé sous l'électrode est rompu, permettant un accès électrique à la cellule. Comparé à l'utilisation d'électrodes pointues, le patch-clamp pour cellule entière permet des enregistrements beaucoup plus précis et, de manière cruciale, est moins dommageable pour la cellule. Cela a permis une étude systématique des processus synergiques au niveau cellulaire, tels que la régulation des courants macroscopiques par des molécules modulatrices et les interactions entre les différents types de canaux dans le neurone.
L'ouverture relativement grande créée dans la cellule dans la configuration de cellule entière donnait également accès à la cellule par des produits chimiques, permettant ainsi aux colorants d'être délivrés pour visualiser les structures cellulaires complexes et d'extraire l'ARN pour l'analyse de l'expression génique.. Le groupe de Neher a examiné la séquence des événements qui sous-tendent le transfert d’informations entre les cellules en introduisant des produits chimiques dans la cellule et en suivant simultanément les modifications des propriétés électriques de la membrane de la cellule..
Le patch-clamp de cellules entières s'est avéré idéal pour étudier les propriétés collectives des neurones et des réseaux neuronaux dans des tranches de cerveau maintenues in vitro. Le fait de travailler avec des systèmes plus complexes, tels que les réseaux neuronaux, présente un défi: le nombre de facteurs de confusion possibles augmente. La solution de Sakmann dans les années 90 consistait à effectuer un enregistrement simultané de cellules entières en utilisant deux ou trois électrodes, ce qui paraissait excessif à certains, car des données comparables pouvaient être obtenues par des enregistrements séquentiels utilisant moins d’électrodes. Cependant, le raisonnement était que prendre du temps pour concevoir l'expérience quasi parfaite atténuait les difficultés ultérieures d'interprétation des données analogues à celles rencontrées par Katz et Miledi.
Par conséquent, des enregistrements simultanés de différentes parties du neurone ont définitivement confirmé que les potentiels d'action sont initiés sur une partie de la protrusion neuronale longue principale (l'axone) et se propagent ensuite vers les dendrites (protrusions en grappes qui reçoivent des entrées d'autres neurones).. Les mécanismes sous-jacents à la signalisation entre neurones ont été directement étudiés en plaçant des électrodes de part et d'autre d'une connexion synaptique. De plus, des enregistrements triples de neurones de différentes classes ont révélé certains principes de base de l'organisation de réseau.
La technique du patch-clamp est également utilisée pour examiner les activités des cellules dans des conditions plus naturelles. Pour étudier la manière dont les stimuli sensoriels et les mouvements sont représentés dans le cerveau, des expériences doivent être effectuées sur des animaux vivants. Le défi avec cette approche, cependant, est que le moindre mouvement peut déloger une électrode du neurone. Le clampage de cellules entières s'avère remarquablement stable en raison de l'étanchéité entre l'électrode et la membrane. Ainsi, cette technique a permis d’enregistrer des dendrites et des paires de neurones chez les rongeurs anesthésiés et même chez les animaux capables de marcher et de courir.
L’enregistrement patch-clamp est sans doute encore le moyen le plus direct et le plus efficace d’étudier les signaux électriques dans le cerveau. Les données obtenues avec cette technique représentent essentiellement la vérité de terrain pour les chercheurs dans de nombreuses branches des neurosciences, de la part de théoriciens. aux chercheurs en translation qui développent des médicaments pour le traitement de certaines affections cérébrales, y compris l'épilepsie et trouble du spectre autistique.
De plus, le patch-clamp complète les techniques «optogénétiques» modernes, qui permettent de contrôler et de visualiser les activités de vastes populations de neurones en utilisant des. Technologies émergentes, telles que les prothèses pour la visionreposera probablement beaucoup sur l’enregistrement patch-clamp pour établir les conditions optimales de conversion des stimuli externes en signaux électriques. Le patch-clamp restera clairement un outil essentiel pour le neuroscientifique dans un avenir proche.
[ad_2]