[ad_1]
Les organelles appelées mitochondries sont les centrales énergétiques de la cellule. En tant que partie cruciale de la machinerie cellulaire, toute perturbation de leur fonctionnement pourrait avoir de graves conséquences. Il existe donc des mécanismes pour lutter contre le dysfonctionnement mitochondrial. Écrire dans La nature, rapportent une voie qui s'attaque aux problèmes d'importation de protéines dans les mitochondries, au fur et à mesure de leur apparition, afin de prévenir les dysfonctionnements mitochondriaux et cellulaires. Cette voie utilise une partie du kit de réparation cellulaire qui traite les protéines endommagées dans un autre organite – le réticulum endoplasmique (ER).
Au moins 1 000 protéines résident dans la mitochondrie de la levure, où elles exercent des fonctions contribuant à la production d'énergie cellulaire et au métabolisme.. Presque toutes ces protéines sont fabriquées dans le cytoplasme et sont ensuite transportées dans les mitochondries sous forme de précurseur non plié. Les mitochondries reçoivent un flux entrant important de flux de protéines, et la voie d’entrée qui porte le poids de cet afflux est un complexe protéique situé à la surface des mitochondries, appelé complexe TOM. Lorsque le complexe de TOM devient surchargé ou est compromis en raison de lésions mitochondriales, les protéines mitochondriales non pliées peuvent s'accumuler dans le cytoplasme et entraîner une toxicité cellulaire.–. Des mécanismes existent pour combattre le stress sur les cellules qui en résulte–, mais comment les mitochondries gèrent-elles l’échec de l’importation de protéines n’est pas clair.
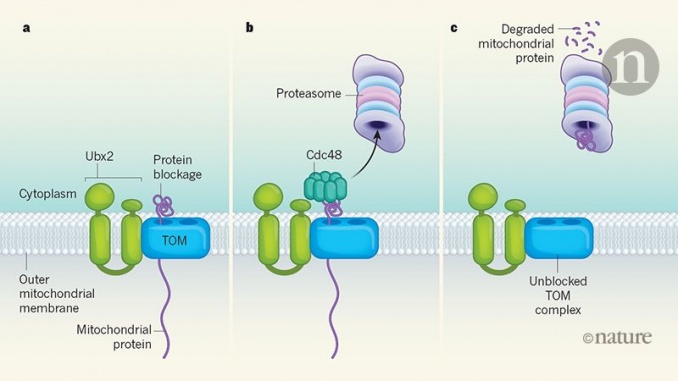
Les pores d'un complexe TOM seront parfois obstrués par une protéine mitochondriale (Fig. 1). Le mauvais repliement des protéines est un événement cellulaire courant qui peut être exacerbé par le stress ou se produire si une protéine se présente sous une forme mutante.. Une protéine précurseur mitochondriale qui se plie prématurément dans le pore du complexe TOM pourrait s'y coincer. Un blocage peut également se produire si les niveaux d'énergie de la cellule chutent, ce qui ralentit ou stoppe l'importation des protéines.. Si une telle obstruction n'est pas supprimée, l'accumulation de protéines précurseurs non pliées dans le cytoplasme peut déclencher des modifications de la transcription conduisant à la libération d'une réponse de stress cellulaire.. Ces voies de réaction au stress, comprennent la voie UPRam et la voie mitoCPR, qui amorcent le système d'élimination des déchets cytoplasmique – un complexe protéique appelé protéasome – afin de dégrader les protéines précurseurs accumulées.
Mårtensson et al. ont examiné si un système était en place pour surveiller en permanence le complexe TOM et éliminer les protéines précurseurs piégées, empêchant ainsi les blocages d'entraver l'importation de protéines dans une mesure générant un stress cellulaire. Un tel système de surveillance est en place pour une porte d'entrée dans l'ER. Pour identifier les facteurs susceptibles d’éliminer les protéines précurseurs piégées, Mårtensson et al. purifié le complexe de TOM de la mitochondrie des cellules de levure. L'une des protéines associées au complexe TOM qu'ils ont identifiées était Ubx2, ce qui était une surprise. En effet, Ubx2 est surtout connu pour son activité à l'urgence, où il intervient dans l'élimination systématique des protéines mal repliées dans le cadre d'une voie de contrôle de la qualité spécifique à l'ER appelée dégradation associée à l'ER (ERAD).,. Mårtensson et ses collègues ont mené des expériences biochimiques qui ont montré qu'Ubx2 existe dans deux pools cellulaires distincts, l'un au niveau de l'ER et l'autre sur la surface mitochondriale associée aux complexes TOM.
Dans la voie ERAD, les enzymes ajoutent l'ubiquitine, une protéine, aux protéines mal repliées qui sont piégées dans l'urgence.,. Cette balise d'ubiquitine est reconnue par Ubx2, ce qui déclenche le recrutement d'une protéine appelée Cdc48, un type d'enzyme appelée AAA ATPase. Cdc48 extrait les protéines mal repliées de l'ER et les transmet au protéasome en vue de leur dégradation,. Pour déterminer si Ubx2 pourrait fonctionner de la même manière dans les mitochondries, Mårtensson et ses collègues ont vérifié si Cdc48 interagissait avec le complexe TOM. Ils ont constaté que c'était le cas et que l'interaction dépendait d'Ubx2. Lorsque les auteurs ont bloqué la source d'énergie nécessaire à l'importation de protéines mitochondriales, cela s'est traduit par une accumulation de protéines précurseurs uniquement dans les mitochondries dépourvues d'Ubx2.
L'accumulation de protéines précurseurs en l'absence d'Ubx2 a également été observée si l'importation de protéines mitochondriales était ralentie par un autre moyen, à savoir l'utilisation d'une version mutante d'une protéine qui entraîne l'importation de protéines dans les mitochondries.,. Dans cette configuration, Mårtensson et al. ont observé que les protéines précurseurs s’accumulaient dans le cytoplasme de cellules présentant des défauts de Cdc48 ou dans un composant du protéasome, ce qui indique que la Cdc48 et le protéasome jouent un rôle clé dans cette voie.
Pour déterminer spécifiquement si Ubx2 est nécessaire pour éliminer les protéines précurseurs qui encrassent le complexe TOM, Mårtensson et ses collègues ont exprimé des protéines précurseurs mitochondriales, dans la levure, qui ont été choisies car elles sont importées lentement dans l'organite. Les auteurs ont conçu ce scénario pour augmenter le nombre d'événements de blocage, puis extrait les complexes TOM. Ils ont découvert que, dans les cellules dépourvues d'Ubx2, les protéines précurseurs étaient bloquées dans des complexes de TOM. Cependant, dans les cellules où Ubx2 était présent, aucune protéine précurseur n'a été détectée dans les complexes de TOM. Cet élément de preuve clé indique qu'Ubx2 fait partie d'un mécanisme de contrôle de la qualité jusqu'alors inconnu, qui surveille le complexe TOM, et Mårtensson. et al. l’ont nommée voie de dégradation associée à la translocation des protéines mitochondriales (mitoTAD).
Les conclusions de Mårtensson et de ses collègues soulèvent deux questions cruciales. Premièrement, quelle est la relation entre la voie mitoTAD et les voies de contrôle de la qualité mitochondriales qui fonctionnent dans des conditions de stress cellulaire? Au cours de leur enquête, les auteurs ont mis au jour un lien fonctionnel entre Ubx2 et la protéine Vms1, ainsi qu’avec l’enzyme Msp1 (qui, comme Cdc48, est une AAA ATPase). Vms1 et Msp1 ont toutes deux été impliquées dans les processus de contrôle de qualité mitochondriaux–. Lorsque les auteurs ont retiré ces protéines de cellules dépourvues d'Ubx2, les mitochondries ont perdu leur fonction de production d'énergie et les protéines marquées à l'ubiquitine se sont accumulées. Ce résultat suggère que Vms1 et Msp1 fonctionnent de manière complémentaire à la fonction Ubx2. Une étude visant à évaluer la diaphonie entre ces voies et la voie mitoTAD pourrait approfondir notre compréhension des mécanismes de contrôle de la qualité des mitochondries.
Deuxièmement, comment Ubx2 reconnaît-il qu'une protéine précurseur est bloquée dans le complexe TOM? Ubx2 peut se lier à l'ubiquitine, c'est pourquoi l'ubiquitine est probablement utilisée pour marquer les protéines précurseurs encrassées. Définir les composants de la machinerie d'ubiquitination et les signaux d'ubiquitine qui régissent non seulement la voie mitoTAD, mais également les voies de contrôle de la qualité induites par le stress qui régulent l'importation de protéines mitochondriales constituera une orientation importante pour les recherches futures. Le fait que le RE et les mitochondries utilisent la même protéine pour le contrôle de la qualité pourrait impliquer que ces processus sont co-régulés.
De nombreuses autres questions fascinantes restent également à traiter. Entre-temps, les travaux de Mårtensson et de ses collègues ont brossé un tableau éclairant d’un aspect jusque-là inconnu de la façon dont les mitochondries protègent leur porte d’entrée principale.
Inscrivez-vous pour le quotidien Briefing Nature Courriel
Restez au courant de ce qui compte dans la science et pourquoi, choisi à la main La nature et d'autres publications dans le monde.
S'inscrire
[ad_2]