[ad_1]
Lorsque Hamlet est mortellement blessé par la lame empoisonnée de Laertes lors d’un match d’escrime, il change d’arme et riposte, de sorte que Laertes soit tué par son propre épée. , Klompe et al. décrire un changement d’arme tout aussi spectaculaire dans la guerre biologique. Ils rapportent qu'une machine moléculaire appelée Cascade, que les bactéries utilisent pour se défendre contre des envahisseurs génétiques, peut également être utilisée contre eux par certains de ces envahisseurs. Pour ajouter au drame, ce minuscule instrument de guerre pourrait éventuellement se trouver servir un objectif pacifique: le génie génétique des cellules humaines pour traiter les maladies.
Les génomes des bactéries sont constamment assaillis par des segments d’ADN «égoïstes» (tels que les gènes de virus infectant les bactéries et d’éléments génétiques mobiles), qui améliorent leur propre propagation et leur transmission plutôt que celles de leur hôte. Un type d'élément mobile s'appelle un transposon. Certains transposons ne portent que cinq gènes dont la seule fonction est de répandre le transposon parmi les bactéries.. Les produits protéiques de ces gènes agissent ensemble pour insérer l’ADN du transposon dans un endroit spécifique du génome d’une bactérie auquel l’insertion ne nuit pas à l’hôte. Le transposon devient ainsi un «passager» permanent de cette bactérie. Lorsque l'occasion se présente, elle se transfère dans l'une des petites pièces d'ADN circulaires que les bactéries transmettent entre elles pour transférer du matériel génétique, et peut ainsi se déplacer vers un nouvel hôte..
Les bactéries sont armées de plusieurs systèmes de défense contre ces parasites. On est connu comme CRISPRet fonctionne de la même manière qu’une affiche «recherchée» d’un criminel. Lorsque de l'ADN étranger pénètre dans une cellule bactérienne, CRISPR la découpe et place quelques fragments dans le génome bactérien. Ces fragments ne sont pas des trophées de guerre qui ramassent la poussière, mais des souvenirs des invasions du passé: la bactérie les copie dans de courts extraits d’ARN et les transmet à des enzymes dédiées à la nucléase associées à CRISPR, dont Cas9 est la mieux étudiée.,. Ces nucléases portent les fragments d’ARN et les comparent à l’ADN entrant; s'il y a une correspondance, l'ADN envahissant est détruit.
En 2017, un fait étrange a été rapporté par Peters et al.: certains transposons portent également des gènes pour Cascade, un type de système de défense CRISPR. Cela n'avait aucun sens. Pourquoi un élément génétique parasite aurait-il besoin d'un mécanisme de défense qui se cible lui-même? Les caractéristiques des êtres vivants ne sont pas toutes des adaptations darwiniennes, mais la surprenante prévalence de Cascade dans les transposons de nombreuses bactéries impliquait qu'il devait être là pour une raison.
Cependant, Peters et al. a noté deux particularités des systèmes Cascade – transposon. Premièrement, bien que la machine Cascade ait encore reconnu un ADN cible en la comparant à un extrait d'ARN porté par une protéine de type Cas, cette machine ne pouvait pas couper l'ADN et ressemblait donc à une arme à feu chargée de blancs. Deuxièmement, le transposon contenait tous les gènes habituels nécessaires pour intégrer son ADN dans un génome bactérien, mais ne possédait pas le gène qui dirige cette intégration vers la destination habituelle «sans danger pour l’hôte» – empêchant ainsi le canon Cascade de viser une cible spécifique. Peters et al. ont émis l'hypothèse que ces deux inconvénients constituent un avantage: le transposon pourrait peut-être utiliser Cascade pour reconnaître un nouvel ADN cible dans une bactérie, puis acheminer l'intégration de l'ADN du transposon vers ce site?
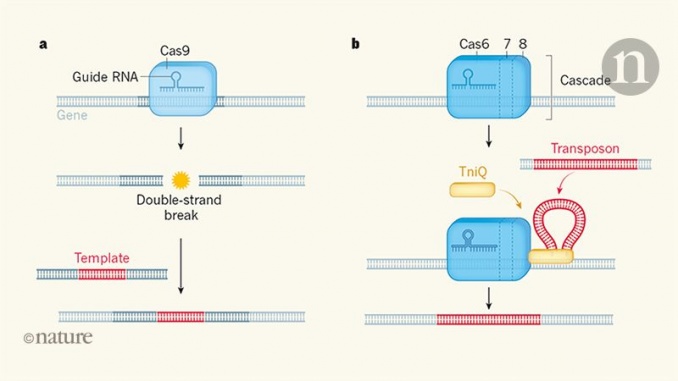
Klompe et ses collaborateurs fournissent maintenant une mine de données expérimentales qui prouvent et développent cette idée. Ils montrent que le transposon peut utiliser la composante guidée par l'ARN de son passager Cascade pour diriger Cascade vers une position particulière dans un génome. Ils rapportent également qu'après la reconnaissance de l'ADN cible, Cascade se lie directement à une protéine (TniQ) qui guide l'insertion du transposon vers le nouvel emplacement du génome (Fig. 1). Cette insertion est extrêmement spécifique: dans les 25 cas étudiés par les auteurs, le transposon a été livré avec précision et exclusivement à l'adresse ciblée dans le génome bactérien. Les conclusions de Klompe et ses collègues illustrent comment l'évolution des microbes peut transformer, mélanger et combiner des composants afin de proposer des solutions radicalement nouvelles aux problèmes, aboutissant dans ce cas à une transposition de l'ADN guidée par l'ARN.
Les travaux inspireront les chercheurs travaillant sur un tout autre domaine scientifique: le génie génétique des êtres humains pour traiter les maladies. Les gènes thérapeutiques sont généralement installés chez l'homme à l'aide de virus qui persistent en dehors du génome de la cellule (ce qui signifie qu'ils sont rapidement dilués lorsque la cellule se divise) ou atterrissent de manière semi-aléatoire dans l'ADN génomique (ce qui soulève des problèmes de sécurité potentiels).. Une solution à ce problème est la technique appelée édition du génome, – dans lequel une nucléase modifiée, telle que Cas9, est destinée à couper l'ADN en une position d'intérêt pour produire une rupture à double brin (DSB), qui est ensuite réparée à l'aide d'un modèle facilitant l'insertion d'un gène à cette position (Fig. 1a).
Bien que l’addition de gènes basée sur le DSB soit utile, elle a ses limites. Premièrement, cela fonctionne de manière relativement inefficace dans les cellules non divisées, dont beaucoup sont des cibles potentielles pour la thérapie génique. Deuxièmement, le gène à insérer doit être flanqué de segments d'ADN correspondant à la séquence de la région du génome dans laquelle il est inséré, ce qui occupe une place précieuse dans l'agent thérapeutique. Et troisièmement, la génération d’un DSB a un risque associé, bien que gérable. Les deux Peters et al. et Klompe et al. suggèrent que les transposons rapportés apportent, en principe, une solution à tous ces problèmes: le processus d'intégration des transposons ne nécessite pas de DSB au niveau de la cible (Fig. 1b), ni d'ADN flanquant dans l'agent thérapeutique, et devrait fonctionner dans des conditions non divisibles. cellules. Par conséquent, cela pourrait être une approche attrayante pour l'édition de gènes humains en clinique.
Cependant, une longue liste de contrôle doit être complétée avant que les applications cliniques puissent être sérieusement considérées. Cette liste comprend: la démonstration que le processus fonctionne efficacement aux positions cibles du génome dans les cellules humaines concernées par la maladie (plutôt que chez les bactéries); démontrer qu'il peut intégrer des fragments d'ADN suffisamment volumineux pour être cliniquement utiles; prouver sa spécificité dans le génome humain, environ 1 000 fois plus volumineux que celui bactérien; et en développant des moyens de délivrer aux cellules le complément complet de protéines associé au processus d'intégration sans déclencher de réponse immunitaire humaine. La charge de travail est considérable, mais l’un des enseignements clés des 30 dernières années de recherche sur la thérapie génique est que la plupart des problèmes de ce type sont finalement résolus.,,. Par conséquent, un système CRISPR utilisé par les transposons pour se propager pourrait bien se retrouver utilisé pour la médecine génétique.
Inscrivez-vous pour le quotidien Briefing Nature Courriel
Restez au courant de ce qui compte dans la science et pourquoi, choisi à la main La nature et d'autres publications dans le monde.
S'inscrire
[ad_2]