[ad_1]
La chimiothérapie agit généralement en induisant des lésions de l'ADN entraînant la mort cellulaire. Cependant, plutôt que de mourir après une chimiothérapie, certaines cellules tumorales entrent dans un état inactif, appelé sénescence, dans lequel elles sont en vie mais ont définitivement cessé de se diviser.. Bien que la sénescence des cellules normales entraîne le vieillissement et la dégénérescence des tissus, la sénescence induite par le traitement du cancer est associée à des résultats cliniques positifs. Comprendre les facteurs qui déterminent la sénescence des cellules tumorales pourrait ainsi contribuer au développement de nouveaux traitements anticancéreux. , Hsu et al. mettre en lumière un aspect jusque-là inconnu du contrôle de l'entrée en sénescence induite par la chimiothérapie.
Bien que de nombreux progrès aient été réalisés pour mettre au jour les facteurs qui conduisent à la sénescence, les processus qui engagent finalement les cellules dans ce destin sont mal compris. Un nombre croissant de preuves indique que la réglementation de l'engagement d'entrer dans la sénescence est complexe. La simple présence de facteurs associés au déclenchement de ce destin cellulaire ne suffit pas, en soi, à fournir un «commutateur» à la sénescence.
La protéine p21 est probablement mieux connue pour son rôle dans le blocage de la division cellulaire en inhibant des complexes protéiques appelés kinases dépendantes de la cycline. En cas de dommages à l'ADN, l'activité de p21 interrompt la division cellulaire et la croissance, donne aux cellules le temps de réparer leur ADN et évite ainsi que de tels dommages aient des conséquences cellulaires catastrophiques. Il existe des preuves que p21 peut induire une sénescence pendant la chimiothérapie. Pourtant, paradoxalement, certaines recherches suggèrent que la protéine peut favoriser la division des cellules cancéreuses après la chimiothérapie.. Une explication possible de cette divergence est que l'abondance et la dynamique de p21 après la chimiothérapie jouent un rôle clé dans la détermination du passage ou non de la sénescence des cellules cancéreuses.
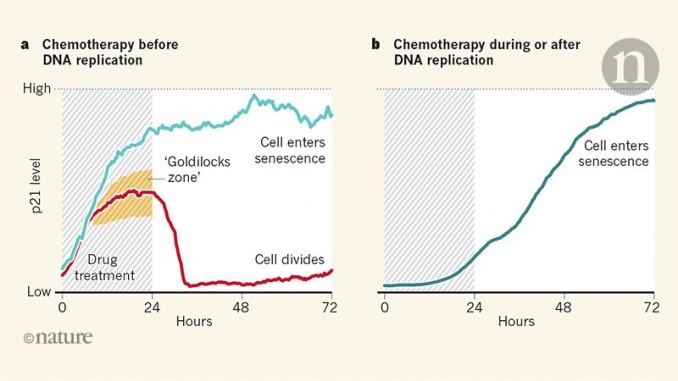
Pour tester cette idée, Hsu et ses collègues ont mis au point un système de microscopie permettant d'étudier des milliers de cellules de cancer du poumon et du côlon humain cultivées, qui avaient été traitées avec un médicament de chimiothérapie endommageant l'ADN. Les auteurs ont surveillé l'abondance de p21 en la marquant avec une protéine fluorescente et ont également suivi la progression des différentes étapes du cycle cellulaire. Contrairement aux recherches précédentes suggérant que des niveaux élevés de p21 conduisent invariablement à la croissance cellulaire ou à la sénescence,, les auteurs décrivent une image complexe, mais unificatrice, de la relation entre les niveaux de p21 et le destin des cellules. Hsu et al. ont noté que si la chimiothérapie entraînait une augmentation initiale des taux de p21 suivie d'un déclin à des niveaux faibles, la division cellulaire avait lieu plutôt que la sénescence (Fig. 1). Les cellules cancéreuses qui sont entrées en sénescence après le traitement médicamenteux avaient initialement un niveau bas de p21 qui a progressivement augmenté pour atteindre un niveau élevé.
Hsu et ses collègues suggèrent qu'il existe une «zone de blocage» pour la prolifération – un niveau de p21 qui est «juste de faire» pour permettre aux cellules tumorales de se diviser après la chimiothérapie. Comment la dynamique de p21 pourrait-elle contrôler le destin des cellules de cette manière? Les médicaments de chimiothérapie sont les plus dommageables pour l'ADN s'ils sont administrés à des cellules au stade du cycle cellulaire au cours duquel la réplication de l'ADN a lieu. On peut donc s’attendre à ce que les cellules traitées par chimiothérapie pendant la réplication de l’ADN présentent des taux de p21 supérieurs à ceux des cellules traitées avant la réplication de l’ADN. Pourtant, de manière surprenante, Hsu et ses collègues ont découvert que les cellules traitées lors de la réplication de l’ADN présentaient des niveaux élevés de dommages à l’ADN mais de faibles niveaux de p21, et que les niveaux de p21 augmentaient ensuite avec le temps. En revanche, le traitement médicamenteux avant la réplication de l'ADN a entraîné une augmentation rapide de l'expression de p21 qui, selon les cellules, est revenue à un niveau bas ou a augmenté davantage.
Comment certaines cellules cancéreuses ayant subi des dommages à l'ADN induits par un médicament peuvent-elles redevenir des niveaux d'expression de la p21 faibles et acquérir la capacité de se diviser? Les auteurs proposent un modèle intégrant une régulation dynamique de l'expression de p21 et du niveau de dommage de l'ADN. Ils suggèrent que le destin des cellules après la chimiothérapie montre une propriété appelée bistabilité – les cellules sont sur le point de suivre l'un des deux destins.
Dans ce scénario, au stade du cycle cellulaire précédant la réplication de l'ADN, si les cellules expriment des niveaux intermédiaires de p21 et que de faibles fluctuations surviennent dans les signaux identifiant les dommages de l'ADN dus à la chimiothérapie, ces fluctuations pourraient favoriser soit l'induction rapide, soit le déclin de l'expression de p21, entraînant le développement des cellules. entrer, respectivement, sénescence ou diviser.
Cependant, lorsque les cellules subissent une réplication de l'ADN, étape du cycle cellulaire au cours de laquelle les signaux de destruction de l'ADN sont supérieurs à la normale (des erreurs pouvant survenir lors de la réplication de l'ADN), seule une légère augmentation du niveau de p21 suffirait à établir un état stable. état de p21 élevé qui conduirait à la sénescence. Ainsi, la zone de Goldilocks est définie par le niveau de p21 et de dommages à l'ADN et détermine si les cellules se divisent après la chimiothérapie. Pour évaluer la pertinence clinique de cette découverte, il convient d’examiner en détail la dynamique et la dépendance à la drogue de la dynamique de p21 au cours de la chimiothérapie.
Ces résultats laissent penser que le ciblage des cellules cancéreuses à des stades spécifiques du cycle de la cellule produirait des différences majeures dans la réponse cellulaire à la chimiothérapie, les cellules ciblées pendant ou peu après la réplication de l'ADN étant plus susceptibles d'entrer en sénescence que les cellules ciblées avant la réplication. Ce modèle devrait être approfondi. Adopter une telle approche en clinique poserait toutefois des problèmes, étant donné que les tumeurs contiennent un mélange de populations de cellules qui se trouvent à différents stades du cycle cellulaire. Une stratégie pour y remédier pourrait consister à orienter les cellules vers le stade spécifique du cycle cellulaire auquel la chimiothérapie serait la plus efficace. Les auteurs ont découvert que si les cellules étaient traitées avec une petite molécule qui déclenche la réplication de l'ADN, la sénescence se produirait plus souvent que la division cellulaire après la chimiothérapie.
Un autre défi sera d'identifier le résultat optimal pour un cancer donné après la chimiothérapie. Bien que la sénescence puisse constituer une réponse idéale à certaines tumeurs, d'autres, plus susceptibles de mourir en réponse à une lésion cellulaire, pourraient être traitées plus efficacement en induisant la mort cellulaire plutôt qu'en déclenchant la sénescence.
Les travaux de Hsu et de ses collègues fournissent une base détaillée pour comprendre ce qui gouverne le destin des cellules cancéreuses après une chimiothérapie. Il est maintenant temps de tirer parti de ces progrès pour déterminer s'il est possible de trouver des stratégies permettant de maximiser l'efficacité de notre arsenal actuel d'agents anticancéreux.
[ad_2]