[ad_1]
Les expériences n'ont pas été randomisées. Les enquêteurs n'étaient pas aveuglés par l'attribution; les enquêteurs ont été aveuglés lors de l'évaluation des résultats.
Souches de souris
Balb / c nu / nu (B6.Cg-Foxn1nu) et Myc (FVB-Tg (ARR2 / Pbsn-MYC) 7Key (c'est-à-dire, souris Hi-MYC5) ont été obtenus des laboratoires Charles River et du National Cancer Institute, respectivement.
Des souris Hi-MYC ont été croisées avec C57BL / 6-Gt (ROSA) 26Sortm1 (eYFP) Cos ou C57BL / 6-Gt (ROSA) 26Sortm1 (HBEGF) Awai/ J souris, qui étaient auparavant croisées avec Tg (DCX-cre / ERT2) 1Mul souris pour générer CreERT2non inductible de la protéine fluorescente jaune améliorée (eYFP) ou du récepteur simien de la toxine diphtérique (DTR) Hbegf) sous le contrôle d'un promoteur DCX (tous obtenus du laboratoire de Jackson). La progéniture qui en résulte, DCX-creERT2; loxp-eYFP Salut-MYC ou DCX-creERT2; loxp-HBEGF Les souris Hi-MYC expriment respectivement eYFP ou DTR dans des cellules exprimant DCX après l'administration de tamoxifène aux souris. Les cellules exprimant le DTR peuvent être éliminées après administration de la toxine diphtérique. Des contrôles respectifs ont également été générés par croisement des trois souches.
Immunodéficient B6.Cg-Foxn1nu +/− Des souris nues hétérozygotes ont également été croisées avec la Tg (DCX-cre / ERT2) 1Mul élevé avec Gt (ROSA) 26Sortm1 (HBEGF) Awai/ J pour épuiser les cellules exprimant DCX en nu / nu des souris
Des souris transgéniques Pten ont été générées par un virus spécifique. Pten suppression (Ptenloxp / loxp) dans les cellules épithéliales de la prostate sous le contrôle du promoteur de la probasine (ARR2Pbsn-cre, PB-cre4)30. Les souris transgéniques PyMT expriment l'antigène T moyen du polyomavirus PyV spécifiquement dans les cellules épithéliales mammaires sous le contrôle du virus de la tumeur mammaire de souris (MMTV)31.
Procédures de la souris
Toutes les expériences in vivo ont été approuvées par le Comité de protection des animaux et de l’utilisation des animaux de notre institution (CEA / DRF / IBFJ / iRCM), autorisé par le Ministère de la recherche français, conformément à l’autorisation APAFIS 652-2015022617149597. Le logement, l’élevage et les pratiques de soin des souris sont conformes aux normes décrites dans les règlements sur le bien-être des animaux et dans le guide pour le soin et l’utilisation des animaux de laboratoire (Directive UE 2010/63).
Pour DCX-creERT2recombinaison induite par le tamoxifène a été préparée dans de l'huile de maïs (100 mg / kg, deux fois par jour pendant 5 jours consécutifs) (Sigma-Aldrich) et injectée par voie intraperitoneale. Pour DCX+ expériences de déplétion cellulaire, la toxine diphtérique (4 μg / kg, Sigma-Aldrich) a été injectée une fois par jour par voie intrapéritonéale 48 h après la dernière injection de tamoxifène, pendant 3 jours consécutifs.
Pour des expériences sur des modèles transgéniques, DCX-creERT2; loxp-EYFP Des souris Hi-MYC ont reçu une injection de tamoxifène à différents moments de la semaine 3 à la semaine 24 après la naissance et ont été sacrifiées 2 semaines après la dernière injection de tamoxifène. Pour les expériences de traçage génétique inductibles, DCX-creERT2; loxp-EYFP Les souris Hi-MYC ont été injectées aux semaines 3 à 4 après la naissance, et les souris ont été euthanasiées 6, 8, 12 et 16 semaines après la naissance. Pour analyses histologiques après DCX+ épuisement des cellules, DCX-creERT2; loxp-HBEGF Les animaux Hi-MYC ont reçu une injection de tamoxifène (semaine 3, semaine 4, semaine 8, semaine 12, semaine 16 après la naissance) et ont été sacrifiés à la semaine 20.
Pour le modèle xénogénique orthotopique, les tumeurs humaines de la prostate ont été induites par des implantations chirurgicales orthotopiques de 1 × 105 Cellules PC3-Luc transformées en Balb / c âgé de 6 semaines nu / nu des souris Trois semaines après l'injection de cellules, les souris ont été randomisées en groupes et ont reçu orthotopiquement un véhicule ou la greffe appropriée de Lin purifiée.–eYFP+ cellules isolées à partir d'une tumeur de la prostate, de bulbes olfactifs ou de tissus SVZ. Pour DCX+ expériences de déplétion cellulaire, 1 × 105 Les cellules PC3-Luc ont été implantées par voie orthotopique dans des injections de tamoxifène. DCX-creERT2; loxp-HBEGF; nu / nu souris (ou cohortes témoins), 2 jours après la dernière injection de toxine diphtérique, avec ou sans la co-transplantation de sous-populations purifiées de Lin–eYFP+ cellules isolées à partir de tumeurs de la prostate DCX-creERT2; loxp-EYFP Modèle de souris Hi-MYC du cancer.
Microdissection de la SVZ, bulbes olfactifs et gyrus dentés du cerveau de souris adulte
Après l'euthanasie, les têtes de souris ont été coupées au-dessus de la région de la moelle épinière cervicale, et une coupure médiale caudo-rostrale a été pratiquée pour retirer la peau de la tête. Le crâne a été pelé vers l'extérieur pour exposer le cerveau. Les bulbes olfactifs ont d'abord été retirés et recueillis dans du milieu RPMI additionné de 10% de FBS (Life Technologies). Ensuite, le cerveau a été mis en rotation pour exposer sa surface ventrale et la SVZ a été isolée au microscope à dissection, en effectuant d'abord une coupe coronale au niveau de la base du chiasme optique, puis en effectuant une seconde coupe juste avant l'hippocampe (Extended Data Fig. 2b), résultant en une coupe coronale à partir de laquelle la SVZ a été recueillie et placée dans un milieu RPMI additionné de 10% de FBS, comme décrit précédemment.46 L'hippocampe contenant le gyrus denté a été disséqué de la partie caudale restante du cerveau47. La surface interne de l'hémisphère cérébral a été placée de haut en bas pour exposer le côté interne de l'hippocampe. Une pointe d’aiguille a été insérée à la limite du gyrus denté et de la corne d’Ammon et glissée superficiellement le long de l’axe septo-temporal de l’hippocampe afin d’isoler le gyrus denté qui a été recueilli dans du milieu RPMI additionné de 10% de FBS.
Dissociation des tissus du cerveau et de la prostate
Avant d'être dissociés, les tissus de la prostate ont été émincés avec une lame de scalpel, puis placés dans un tube de C pour dissociation enzymatique. Les tissus du cerveau et de la prostate ont été dissociés enzymatiquement en suspensions monocellulaires dans des tubes douceMACS C en utilisant les kits de dissociation des tissus neuronaux (T) ou tumoraux respectifs et l'octo-dissociateur douceurMACS avec éléments chauffants. Les programmes douxMACS NTDK_1 ou m_TDK_1 ont été appliqués, respectivement, conformément aux recommandations du fabricant (Miltenyi Biotec). Après dissociation, la suspension cellulaire a été appliquée sur un entraîneur intelligent MACS (70 μm), centrifugée et remise en suspension dans un tampon de fonctionnement MACS.
Culture de cellules
Des cellules PC3 transfectées de manière stable avec le gène de la luciférase 2 sous le contrôle du promoteur de l'ubiquitine C humaine (numéro de catalogue: 128444 / PC-3-luc2, Perkin Elmer) ont été cultivées dans du milieu F12-glutamax supplémenté avec 10% de FBS, 1,5 g / l de bicarbonate sodium (Life Technologies). L'authentification des cellules PC3 a été réalisée par Perkin Elmer (source de la lignée parentale ATCC CRL-1435TM). Toutes les lignées cellulaires fournies par Perkin Elmer sont confirmées exemptes d'agents pathogènes par le profil IMPACT I (PCR) du laboratoire de diagnostic et d'investigation sur les animaux de recherche de l'université du Missouri.
Après dissociation enzymatique des bulbes olfactifs et des cellules de la prostate de DCX-creERT2; loxp-eYFP Souris Hi-MYC, les cellules ont été lavées, remises en suspension dans un milieu neuro MACS (Miltenyi Biotec), puis6 Les cellules ont été étalées dans un puits d’une plaque de culture tissulaire à 24 puits (Thermo Fisher Scientific) préalablement recouverte de polyéthylène.l-ornithine (10 μg / ml, Sigma-Aldrich) et laminine (10 μg / ml, Corning Life Sciences). La moitié du milieu a été remplacée toutes les 48 heures pendant 1 semaine. Ensuite, les cellules adhérentes ont été recueillies et passées sur du poly-l-glithine- et laminine-revêtu de laminine-8 puits (Ibidi). Les cellules ont été incubées dans un milieu neuro MACS additionné de bFGF (20 ng / ml; Preprotech) et d'EGF (20 ng / ml; Preprotech) ou d'un facteur neurotrophique dérivé du cerveau (BDNF, 1 μg / ml, Miltenyi Biotec) et de la neurotrophine-3 ( NT-3, 0,1 µg / ml; Miltenyi Biotec). Le milieu a été remplacé toutes les 48 heures jusqu'à la différenciation neuronale des cellules.
Imagerie de bioluminescence
L'imagerie par bioluminescence in vivo et ex vivo a été réalisée et analysée à l'aide d'un système d'imagerie IVIS série 200 (Xenogen, Caliper Life Sciences). Le signal bioluminescent a été induit par l’injection intrapéritonéale de ré-luciférine (150 mg / kg dans du PBS) 7 min avant l’imagerie in vivo. Pour l'imagerie ex vivo, ré-luciférine (300 mg / kg) a été injectée 8 min avant l'autopsie. Les organes d’intérêt ont été plongés dans une solution de ré-luciférine à 150 mg / ml. Le développement et la progression de la maladie ont été surveillés de très près et les souris métastatiques ont été euthanasiées dès que nous avons constaté des signes de gêne chez la souris, conformément à notre protocole approuvé par IACUC (le signal bioluminescent n'excède pas 1012 photons par s). Dans aucune des expériences, ces limites n'ont été dépassées.
Histologie et immunofluorescence
Pour les coupes incluses en paraffine, les tissus de la prostate chez l’homme et chez la souris étaient préalablement fixés dans du formol ou du paraformaldéhyde à 4%, respectivement. Les blocs ont été sectionnés en série (épaisseur de 5 µm) et la coloration à l'hématoxyline et à l'éosine (H & E) a été réalisée à l'aide de procédures standard. Avant la coloration, les sections ont été déparaffinées avec du xylène et réhydratées par des lavages à l'alcool, puis par récupération de l'antigène dans un tampon au citrate de sodium conformément aux recommandations du fabricant (Vector Laboratories).
Pour les coupes congelées, les souris ont été anesthésiées avec de l'isoflurane à 4% avant de recevoir une dose mortelle de pentobarbital (60 mg / ml). Les souris ont ensuite été fixées par perfusion cardiaque avec 0,9% de NaCl, puis avec du paraformaldéhyde (PFA) à 4% glacé dans du PBS 0,01 M. Le cerveau et la prostate ont été collectés, post-fixés pendant une nuit dans du PFA à 4% à 4 ° C et transférés dans une solution de saccharose à 12% dans du PBS avant la congélation rapide et la coupe au cryostat (épaisseur de 12 µm; Leica).
Pour immunofluorescence, la liaison non spécifique a été bloquée avec du sérum de chèvre dans une solution de BSA, et des coupes ont été incubées pendant une nuit avec des anticorps de souris anti-DCX (Millipore), anti-PSA-NCAM (ABC Scientific) ou anti-cytokératine (Sigma-Aldrich), avec des anticorps de lapin à la MAP-2 (Millipore), à la βIII-tubuline (Covance), à l'α-internexine (Millipore), à la tyrosine hydroxylase (Millipore) ou à l'albumine (GeneTex), à des anticorps de rat anti-CD31 (BioLegend) ou à des anticorps de poulet NF-H (Millipore) ou à eYFP (Aves Laboratories). Une coloration secondaire a ensuite été réalisée pendant 1 heure à la température ambiante avec les anticorps de chèvre Alexa Fluor 647, 568 ou 488 appropriés conjugués aux IgG de souris, de lapin, de rat et de poulet, respectivement (Life Technologies).
Pour l'administration de colorant, l'albumine marquée à la fluorescéine (65 kDa, 2 mg dilué dans 0,1 ml de solution saline; Sigma-Aldrich) et le dextran marqué au TRITC (4,4 kDa, 2 mg dilués dans 0,1 ml de solution saline, Sigma-Aldrich) étaient simultanément intraveineux et intra-péritonéal. injecté à des souris Hi-MYC âgées de cinq mois sous anesthésie. Après une période de circulation d'une heure, les souris ont été profondément anesthésiées avec de l'isoflurane et du pentobarbital et ont été euthanasiées par perfusion transcardiale avec 0,9% de NaCl, suivie de 4% de PFA glacé dans du PBS 0,01 M. Les cerveaux ont été recueillis, post-fixés pendant une nuit dans du PFA à 4% à 4 ° C et transférés dans une solution de saccharose à 12% dans du PBS avant la congélation rapide et la coupe au cryostat (épaisseur de 14 µm; Leica).
Des images en champ clair de sections complètes de prostate Hi-MYC ont été capturées et collectées avec un axioscan Z1 Zeiss (Zeiss MicroImaging) équipé d'une caméra couleur Hitachi HV-F202FCL contrôlée par le logiciel de microscope Zen.
Les images de fluorescence ont été capturées et analysées à l'aide d'un microscope confocal Leica TCS SP8 X équipé d'un laser à lumière blanche, d'un détecteur confocal PMT SP couplé à un détecteur hybride Leica pour l'imagerie confocale super sensible (Leica). Les images ont été obtenues sous forme de piles 3D balayant toute l'épaisseur du tissu contrôlée par le logiciel LAS X 2.0.1.14392 et analysées à l'aide du logiciel d'imagerie 3D haute performance Volocity 6.3.1 (Perkin Elmer).
Échantillons de prostate humaine
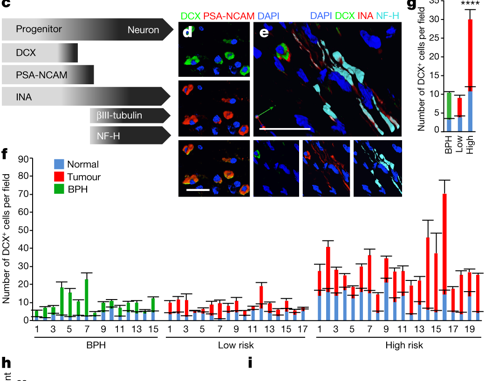
Les prostatectomies radicales ont été obtenues pour la coloration après l'approbation du comité d'examen institutionnel par la plateforme du département de pathologie et ressources biologiques de l'hôpital Henri Mondor (CPP n ° 16169). Avant de signer le formulaire de consentement, tous les patients ont été informés du protocole et du point de vue de la confidentialité, et tous les échantillons recueillis ont été anonymisés avec un numéro d’identification avant d’être publiés à des fins de recherche clinique. Les tissus humains de la prostate ont été collectés, fixés dans du formol et incorporés dans de la paraffine dans le cadre des soins de routine à l'hôpital Henri Mondor (protocole n ° DC2009-930). Pour chaque bloc, une section a été colorée avec H & E afin d'évaluer la viabilité des tissus, de localiser les zones normales parmi les cancers et de cartographier les différentes zones de grade de Gleason. Tous les patients avaient un cancer de la prostate ou une hyperplasie bénigne histologiquement et localement localisé, et n'avaient pas reçu de traitement préalable dans l'établissement. Les caractéristiques du patient, y compris l'âge, les taux d'antigène spécifique de la prostate (PSA) préopératoires, la date de l'intervention chirurgicale, les stades pathologiques et le score de Gleason, sont présentées dans le tableau complémentaire 1. La récurrence du PSA est définie comme une valeur de PSA unique à> 0,2 ng / ml, 2 valeurs à 0,2 ng / ml, ou traitement secondaire pour un PSA en hausse. La récidive peut être locale ou distante, bien qu'aucune métastase n'ait été documentée jusqu'à présent dans cette cohorte de patients. L'extension extra-prostatique a été définie comme une maladie impliquant une ou plusieurs extensions extracapsulaires, ganglionnaires ou vésiculaires séminales et des marges chirurgicales positives. Quantification de DCX+ les cellules ont été réalisées à l'aveugle (sans connaissance des données cliniques) dans les tumeurs de la prostate ou les zones hyperplasiques et dans les tissus restants de la prostate normaux entourant les zones de cancer. Pour chaque marqueur défini ci-dessus, une moyenne de 10 champs représentatifs (un champ = 0,15 mm2) a été calculé pour les zones normales et pour le grade de tumeur capturé comme décrit ci-dessus. Un total de 1.040 zimages empilées ont été acquises et converties en projections 2D maximales analysées avec le logiciel Volocity pour quantifier DCX+/ DAPI+ cellules par champ (DAPI, 4 ', 6-diamidino-2-phénylindole).
Cytométrie en flux
Le cerveau et la prostate de DCX-creERT2; loxp-eYFP Les souris Hi-MYC ont été disséquées et dissociées comme décrit ci-dessus. La cellularité de la SVZ, les bulbes olfactifs, le gyrus denté et la prostate ont été comptés manuellement avec une viabilité au bleu trypan à l'aide d'une chambre de Neubauer avant l'analyse du flux.
Ensuite, 106 les cellules ont été incubées pendant 10 minutes avec du réactif bloquant FcR (Miltenyi Biotec). Ensuite, des anticorps monoclonaux conjugués à un fluorochrome spécifiques de CD45 de souris (clone 30F11), TER119 (clone Ter-119), CD31 (clone 390), CD326 (clone caa7-9G8), CD49f (clone REA518), SCA-1 (clone REA422), SCA-1 (clone REA518), ), PSA-NCAM (clone 2-2B), CD24 (clone M1 / 69) ont été utilisés pendant 20 min à la concentration recommandée par les fabricants (Miltenyi Biotec et BioLegend). Les cellules ont également été incubées avec un EGF biotinylé complexé avec de la BV785-streptavidine (Invitrogen, Thermo Fisher Scientific). Les analyses des suspensions de cellules colorées ont été effectuées sur un SORP LSR II à 5 lasers (355/408/488/561/640; BD BioSciences) et les données ont été analysées avec le logiciel FlowJo (Tree Star). Le nombre absolu de cellules a été calculé comme ((nombre de Lin–eYFP+ cellules acquises × cellularité de l'organe) / nombre de cellules individuelles vivantes acquises).
Extraction d'ARN, PCR transcriptase inverse et PCR quantitative
Les niveaux d'expression génique ont été analysés à partir d'ARN extrait, à l'aide de la solution de RLT (Qiagen), à partir de cellules purifiées isolées du cerveau âgé de 8 semaines ou de la prostate âgée de 16 et 52 semaines. DCX-creERT2; loxp-eYFP Salut-MYC souris par PCR quantitative en temps réel. La transcription inverse (exposant VILO; Invitrogen) a été réalisée conformément aux instructions du fabricant. La PCR quantitative a été réalisée avec Fast SYBR Green (ABI Applied Biosystems, Thermo Fiscer scientific). L'expression de glycéraldéhyde-3-phosphate déshydrogénase (GAPDH) a été utilisée comme standard. Les séquences d’amorces sont présentées dans le tableau supplémentaire 6.
Séquençage d'ARN
Lin–eYFP+ les cellules ont été isolées à partir de cerveau de 8 semaines ou de prostate de 16 semaines DCX-creERT2; loxp-eYFP Les souris Hi-MYC ont été recueillies à Qiazol (Qiagen). L'ARN a été extrait à l'aide du micro-kit miRNeasy (Qiagen) et des banques d'ARNm ont été préparées à l'aide d'ARN à entrée ultra-basse Smart-Seq v4 (Takara). En résumé, l’ADNc a été synthétisé en utilisant la technologie des acides nucléiques verrouillés (LNA) intégrée à la technologie SMART (mécanisme de commutation à l’extrémité 5 ’de la matrice d’ARN). Pour chaque banque, le nombre de cycles après PCR avec transcription inverse (RT – PCR) a été ajusté en fonction du nombre de cellules. Les bibliothèques ont été adaptées et indexées individuellement à l'aide du kit Illumina Nextera XT, puis contrôlées sur le bioanalyseur Agilent (Tapestation 2200, Agilent Technologies). Les bibliothèques identiques ont été regroupées avant séquençage à une profondeur de lecture moyenne de 70 millions de lectures par échantillon. Les bibliothèques finales ont été contrôlées sur Tapestation 2200 (Agilent Technologies) et ont été quantifiées avec un intercalant fluorimétrique. Toutes les banques de séquençage d'ARN ont été séquencées à l'aide de la cartouche Illumina Nextseq 500 avec HighOutPut afin de générer environ 2 × 400 millions de lectures à 75 bases.
Les lectures séquencées ont été ajustées à l'aide de la version trimmomatic 0.36 basée sur un seuil de qualité de 33. Les lectures ont été alignées sur le Mus musculus libération du génome GRCm38.p6 en utilisant l’aligneur STAR ultra-rapide de RNA-seq. La quantification de l'expression des gènes a été réalisée à l'aide de HTSeq version 0.10 sur la base de paramètres par défaut et des analyses transcriptomiques ont été réalisées avec le progiciel EdgeR. Les identificateurs de terme Ont. De gènes (GO) #GO: 0043005 et #GO: 0030182 ont été sélectionnés pour étudier une liste de gènes associés à la projection et à la différenciation de neurones. Un regroupement hiérarchique dans les représentations de la carte thermique a été généré sur la base de la distance de Ward 2 et de la méthode de couplage complet. Les analyses de corrélation limitées aux listes sélectionnées de gènes appartenant à Gene Ontology ont été effectuées à l'aide du coefficient de corrélation de Spearman, et la signification statistique a été déterminée sur la base des facteurs de corrélation associés. P valeur. L'analyse d'expression de gènes dans 53 populations du projet ImmGenological Genome Project (ImmGen) répertoriées dans le tableau supplémentaire 5 a été réalisée à l'aide du portail Web ImmGen (basé sur le service MyGeneSet). Des comparaisons statistiques entre des échantillons de SVZ, de bulbes olfactifs ou de prostate et des populations ImmGen ont été effectuées sur la base du coefficient de corrélation de Spearman, limité aux listes des 200 gènes les plus fortement exprimés dans chaque échantillon.
Injection stéréotaxique
L'ADNc de tdTomato a été clone sous le contrôle du promoteur CAG dans un plasmide navette lentiviral qui contient un génome auto-inactivant dérivé du VIH-1. Des particules lentivirales recombinantes ont été produites par transfection transitoire de cellules HEK-293T et titrées par dosage ELISA (enzyme-linked immunosorbent assay) de la protéine de capside p24 (HIV-1 antigène p24 ELISA). Avant l’injection dans la SVZ de souris Hi-MYC âgées de 5 semaines, les particules virales ont été diluées dans une solution saline tamponnée au phosphate à une concentration finale de 50 ng de p24 µl.−1 et délivré dans un volume de 2 µl par injection stéréotaxique aux coordonnées suivantes: +0,7 mm antérieur et +1,3 mm latéral par rapport au bregma; et −2,5 mm sous la surface du crâne. La solution virale a été injectée à une vitesse de 0,2 µl.min−1 et la canule d'injection a été laissée en place pendant 5 min avant d'être retirée lentement. Le vecteur rétroviral a été injecté dans le gyrus denté par stéréotaxie aux coordonnées suivantes: 2 mm postérieur et 1 mm latéralement par rapport au bregma; et 2 mm sous la surface du crâne.
Des souris Pten, PyMT et nude ont été injectées par stéréotaxie dans la SVZ avec le vecteur rétroviral décrit ci-dessus aux coordonnées suivantes: +1 mm antérieur / postérieur et ± 1,3 mm latéral par rapport au bregma; et −2,5 mm en dessous de la surface du crâne.
analyses statistiques
Pour les analyses de souris, toutes les valeurs sont rapportées en moyenne + s.e.m. La signification statistique a été évaluée par un élève paramétrique t-tester. La signification a été fixée à P <0,05. Les analyses statistiques ont été réalisées avec GraphPad Prism (, v.7).
Pour les études de patients, des analyses statistiques ont été effectuées à l'aide du logiciel R (R Development Core Team, v.3.3). Les comparaisons statistiques des groupes ont été effectuées à l'aide de tests de Wilcoxon. La non-influence de l'âge des patients sur les comparaisons statistiques a été vérifiée à l'aide d'analyses de régression. Corrélation entre le nombre de DCX+ les cellules et le nombre de zones envahies ont été identifiés à l'aide du coefficient de corrélation de Spearman. Les courbes de survie ont été modélisées à l'aide d'estimations de Kaplan – Meier. La signification statistique de la différence entre les courbes de survie a ensuite été évaluée à l'aide du test log-rank (Mantel – Cox).
La normalité des données a été évaluée à l'aide du test de Shapiro-Wilk. Tous les tests statistiques utilisés étaient bilatéraux. P les valeurs inférieures à 0,05 ont été considérées comme significatives.
Résumé du rapport
De plus amples informations sur la conception de la recherche sont disponibles dans le Résumé du rapport de recherche sur la nature lié au présent document.
[ad_2]